В биоинженерии наступил важный этап: исследователи успешно продемонстрировали возможность 3D-печати сложных объектов непосредственно внутри живых клеток. Эта технология позволяет ученым выйти за рамки простого наблюдения за клетками и перейти к активному «строительству» внутри них, обеспечивая уровень точности и контроля, который ранее считался невозможным.
Технология: двухфотонная полимеризация
Команда под руководством доцента Матьяжа Хумара из Люблианского университета использовала высокоточный метод, известный как двухфотонная полимеризация.
В отличие от традиционной 3D-печати, которая выстраивает слои снизу вверх, этот метод использует высокосфокусированный лазер для отверждения жидкой смолы в определенных микроскопических координатах. Процесс выглядит следующим образом:
1. Биосовместимая жидкая смола вводится в человеческую клетку.
2. Прецизионный лазер воздействует на конкретные точки, превращая жидкость в твердые структуры менее чем за 10 секунд.
3. Оставшаяся незатвердевшая смола растворяется и вымывается в течение двух часов.
Этот метод позволяет достичь разрешения до 100 нанометров — что примерно в 200 раз меньше среднего размера человеческой клетки, — что дает возможность создавать невероятно сложные микроструктуры.
Новые горизонты в исследовании клеток
Чтобы понять значимость этого прорыва, необходимо рассмотреть ограничения предыдущих методов. Исторически у ученых было два основных способа введения объектов в клетки:
* Микроинъекция: физическое прокалывание клеточной мембраны, что часто наносит фатальные повреждения.
* Эндоцитоз: использование естественной способности клетки «поглощать» инородные объекты, что происходит нестабильно и ограничено очень мелкими предметами (менее 1 микрометра).
Печатая объекты in situ (на месте), исследователи обходят эти препятствия. Исследование подтвердило, что процесс удивительно бережен: таймлапс-съемка показала, что клетки, содержащие напечатанные объекты, продолжали вести себя нормально и даже передавали эти объекты своим «дочерним клеткам» во время деления.
От крошечных слоников до биологических штрих-кодов
Чтобы проверить пределы своей точности, исследователи напечатали самые разные объекты — от причудливых фигурок до высокофункциональных структур:
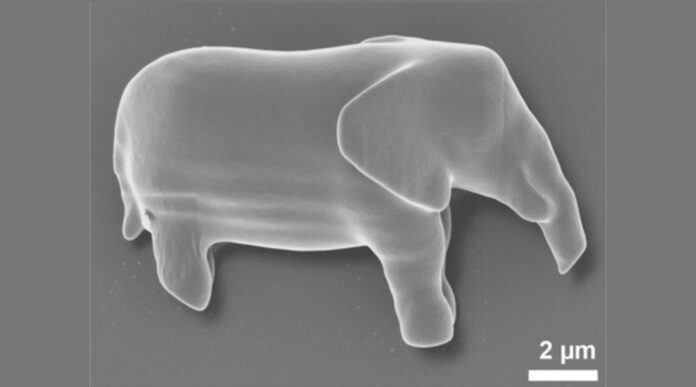
- Доказательство детализации: они напечатали 10-микронную фигурку слона с узнаваемыми чертами, такими как хобот и бивни, чтобы доказать высокое разрешение принтера.
- Клеточная штрих-кодировка: команда создала систему «штрих-кодов» с помощью сетки из цилиндров. Благодаря более чем квинтиллиону возможных комбинаций, эта система может уникально идентифицировать отдельные клетки. Это позволяет ученым отслеживать поведение каждой отдельной клетки, а не полагаться на «средние» данные, полученные от больших, неразличимых популяций клеток.
- Внутренние микролазеры: исследователи попытались напечатать функциональные микролазеры, добавив флуоресцентный краситель в смолу. Хотя это подтвердило концепцию «зондирования» клетки изнутри, сам краситель оказался токсичным, что подчеркивает текущую проблему поиска баланса между функциональностью и жизнеспособностью клеток.
Путь вперед: на пути к внутриклеточным микророботам
Этот прорыв знаменует начало новой эры в интрацеллюлярной биоинженерии. Последствия для медицины и биологии огромны. Будущие области применения могут включать:
- Механические инструменты: печать крошечных рычагов, пружин или барьеров для физического изменения формы или движения клетки.
- Микросенсоры: создание внутренних устройств, которые в режиме реального времени отслеживают уровень pH, температуру, содержание сахара или магнитные поля.
- Биоробототехника: долгосрочное видение предполагает создание микроскопических роботов, способных выполнять задачи внутри клеточной среды.
«Мы закладываем фундамент для нового класса инструментов и методов применения внутриклеточной биоинженерии», — отмечает Матьяж Хумар.
По мере продвижения исследований основной упор будет сделан на разработку специализированных нетоксичных смол, которые максимально увеличат функциональность напечатанных объектов, обеспечивая при этом абсолютную безопасность живого организма.
Заключение: Успешно научившись печатать внутри живых клеток, ученые превратились из простых наблюдателей биологических процессов в активных архитекторов микроскопического мира, прокладывая путь к беспрецедентной точности в клеточной медицине и инженерии.